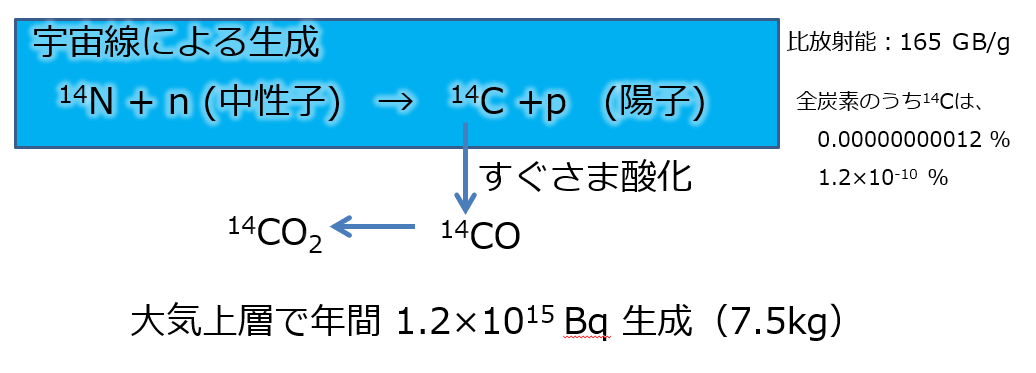
地球を構成する元素のうち、炭素(カーボン)はおよそ0.01%を占めます。地球表層の大気には二酸化炭素として0.04%ほど存在します。放射線を出さずに安定しているのはカーボン12(12C)とカーボン13(13C)です。放射線を出して、半減期が約5700年なのが、カーボン14( 14C )です。カーボン全体の割合としては非常に少ないですが、カーボン14が放つ特有の放射線(β線)で検出することができます。また、加速器質量分析計で環境試料中の14Cを計ることもあります。
カーボン14は絵画や遺跡などの年代測定として使われています。絵画の場合、絵の具は植物などから抽出して作ります。そこにはカーボン12、13、14が一定の割合で存在しています。カーボン12や13の割合は変わりませんが、カーボン14だけは時が経つにつれ減少していきます。減少することで、それぞれの同位体の割合が変化しますので、その割合の変化から年代を推定します。
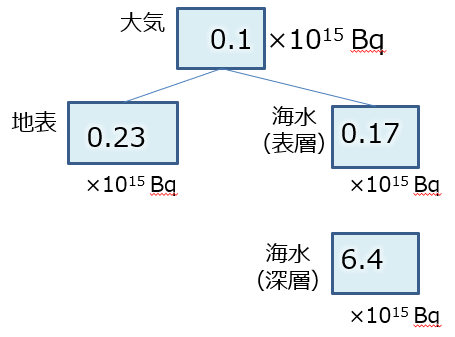
大気上層で生成されたカーボン14 (14C)は二酸化炭素として存在します。大気下層の二酸化炭素は海洋表層の水に溶け込みます。下の絵に、大気と表層海水、深層海水での14C量をまとめました。海水には多量の二酸化炭素が溶け込むので、ボリュームの大きな深層海水に含まれる14Cが最も多くなっています。14Cは大気から供給されるだけなので、深層水では14Cは放射壊変により減り続けます。安定炭素と14Cの割合を測定することで、海水が沈み込んで深層水となった年齢(滞留時間)を推定できます。このような古い海水が、北太平洋で湧昇で表層に運ばれることで、北太平洋表層の14C割合は陸上と比べて小さくなっています。14C年代推定値では数百年の違いが生じています。その海水で育った海洋生物の14C年代推定値も400年ほどずれているといわれています。