クロマトグラフィーとは、化学成分の吸着と脱離の性質を利用した分離手法のことです。炭酸カルシウムを充てんしたカラムに石油エーテルを流すと、色の異なる吸着帯として分離されたことが、クロマトグラフィーのはじまりです。このことから”色の記録”という意味で、ギリシャ語のChroma(色)とGraphos(記録)より Chromatography(クロマトグラフィー)と呼ばれるようになりました(西川計測のHP情報より引用)。
クロマトグラフとは、クロマトグラフィーの装置のことです。
クロマトグラムとは、クロマトグラフ(装置)により分離計測された、信号強度の時系列変化図です(あとで説明します)。
イオンクロマトグラフィーは、水中のイオン成分を分離・分析する手法です。
ガスクロマトグラフィーは、気相中の成分を分離・分析する手法です。
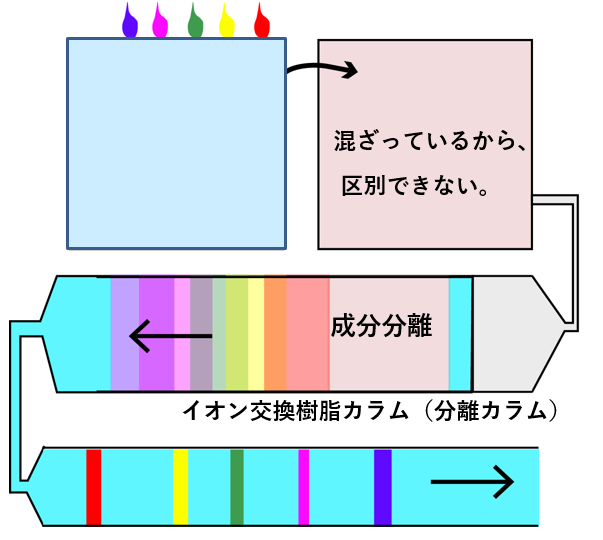
下に、イオンクロマトグラフィーを例に、分離分析のイメージを示します。水に、複数種類の成分が混ぜます。複数種類を色の違いで表現しています。混ざってしまうと。何の成分がどれだけ入っているのか分かりません。混合溶液をイオン交換樹脂カラムに通します。成分ごとにカラムを通過する時間が異なることを利用して、カラムから出てきたときには成分ごと(色ごと)に分離するのです。液体の流れに沿って成分が分離されていて、その下流に検出器を置きます。その信号強度をモニターすれば、各成分の濃度を定量できる仕組みです。
検出器の種類は様々です。イオンクロマトグラフィーであれば、一番シンプルなのが電気伝導度です。濃いイオン成分が流れてくれば、電気伝導度が上がります。蛍光検出器もあります。光を吸収して蛍光を発する成分を高感度で検出することができます。